L'antimoine pour les batteries
Des chercheurs de l'ETH Zurich et de l'Empa ont été les premiers à produire des nanocristaux d'antimoine uniformes. Lors de tests sur des batteries de laboratoire, ceux-ci peuvent non seulement stocker de très nombreux ions lithium, mais aussi des ions sodium. Ce nanomatériau serait donc une alternative prometteuse pour les électrodes des futures batteries à grande capacité de charge.
La chasse est ouverte. Et plus précisément pour de nouveaux matériaux destinés à la prochaine génération de batteries, qui remplaceront un jour les accumulateurs lithium-ion. Ces derniers fournissent aujourd'hui de l'électricité fiable pour les smartphones, les ordinateurs portables et de nombreux autres appareils électroniques portables. Mais l'électromobilité et le stockage stationnaire de l'énergie exigent des batteries plus nombreuses et plus performantes, et la forte demande en lithium qui en découle pourrait entraîner une pénurie de cette matière première. C'est pourquoi on demande des batteries dont la conception est identique à celle des batteries aux ions lithium, mais qui sont basées sur les ions sodium. Bien que des recherches soient menées à ce sujet depuis 20 ans déjà, on en sait étonnamment peu à ce jour sur les matériaux capables de stocker efficacement les ions sodium.
Une électrode en antimoine ?
Dans leur quête de matériaux alternatifs pour les batteries, des chercheurs de l'ETH Zurich et de l'Empa, sous la direction de Maksym Kovalenko, ont peut-être fait un pas en avant : Ils sont les premiers à avoir réussi à synthétiser des nanocristaux d'antimoine uniformes. En raison de leurs propriétés particulières, ceux-ci se prêtent à l'utilisation comme matériau d'anode, aussi bien pour les ions lithium que pour les ions sodium. Les résultats de leur étude viennent d'être publiés dans Nano Letters.
Depuis longtemps, l'antimoine est considéré comme un matériau d'anode prometteur pour les batteries lithium-ion performantes, car ce semi-métal présente une capacité de charge deux fois plus élevée que le matériau d'anode actuellement utilisé, le graphite. Les premières études ont montré que l'antimoine pourrait convenir aux batteries rechargeables au sodium et aux batteries lithium-ion, car il peut stocker les deux ions. Le sodium est une alternative possible plus avantageuse que le lithium, car il est naturellement beaucoup plus abondant et plus uniformément réparti sur la terre que le lithium.
Les nanocristaux ont des avantages
Cependant, pour que l'antimoine obtienne cette grande capacité de stockage, il doit être mis sous une forme spéciale. Kovalenko et son équipe ont mis au point une méthode permettant de synthétiser des nanocristaux uniformes. Les chercheurs sont ainsi parvenus à produire des nanocristaux d'antimoine monodisperses dans des classes de taille de 10 et 20 nanomètres.
Les nanocristaux présentent des avantages décisifs par rapport aux cristaux plus grands. L'antimoine est soumis à d'importantes variations de volume lors de la charge et de la décharge des ions. Dans le cas des nanocristaux, ces changements de volume sont réversibles et se produisent rapidement. En revanche, l'antimoine "normal" deviendrait fragile. Autre avantage important : les nanoparticules d'antimoine peuvent être mélangées à un matériau de remplissage conducteur en carbone. Cela empêche les nanoparticules de s'agglomérer.
Candidat de choix pour le matériau d'anode
Des tests en laboratoire ont montré à Kovalenko et à ses collaborateurs que les électrodes en nanocristaux d'antimoine ont des performances équivalentes pour les deux types d'ions. Les nanoparticules d'antimoine sont donc particulièrement adaptées à l'utilisation dans les batteries à ions sodium, car les matériaux stockant le mieux le lithium jusqu'à présent, le graphite et le silicium, ne fonctionnent pas avec le sodium.
Des nanocristaux très uniformes - seuls 10 pour cent ou moins de leur taille s'écartent de la taille moyenne des particules - ont également permis aux chercheurs de déterminer le meilleur rapport taille/performance. Les chercheurs ont constaté que les nanocristaux d'antimoine de 20 nanomètres offraient les meilleures performances. Si les particules sont de 10 nanomètres ou plus petites, le rapport volume/surface devient défavorable et elles s'oxydent rapidement. En revanche, les cristaux de plus de 100 nanomètres sont détruits par les changements de volume mentionnés lors de la charge et de la décharge.
Une alternative plus coûteuse
Une alternative aux batteries lithium-ion actuelles est-elle donc à portée de main ? Kovalenko fait signe que non. La production de nanocristaux d'antimoine uniformes en quantité et en qualité suffisantes est encore trop coûteuse, bien que le procédé soit en soi relativement simple. "Globalement, les batteries utilisant des ions sodium et des nanocristaux d'antimoine comme matériau d'anode ne constituent une alternative prometteuse aux batteries lithium-ion actuelles que si les coûts de fabrication de la batterie et les performances du stockage d'électricité sont comparables", conclut Kovalenko.
Une autre conclusion importante de cette étude est qu'il n'est pas si important d'utiliser des nanoparticules ultra-uniformes dans une électrode pour obtenir des performances élevées. L'antimoine est relativement "docile". En effet, les chercheurs ont également découvert que des particules de 20 à 100 nanomètres pouvaient être utilisées sans que la densité énergétique ou les taux de décharge et de charge n'en souffrent. D'autres matériaux testés par les chimistes sont moins tolérants à cet égard. Si la taille de leurs particules augmente, ces caractéristiques de performance diminuent fortement. L'antimoine occupe donc une position unique parmi les matériaux qui se combinent avec le lithium et le sodium.
"Cela simplifie considérablement le développement d'une synthèse économiquement réalisable pour la formation des cristaux", souligne le professeur de l'ETH. C'est d'ailleurs la prochaine étape de son groupe, en collaboration avec son partenaire industriel, pour trouver une méthode de synthèse plus avantageuse. Kovalenko estime qu'il faudra au moins dix ans avant qu'une batterie au sodium avec une électrode antimoine puisse être mise sur le marché. La recherche dans ce domaine n'en est qu'à ses débuts.
Piles au lithium-ion
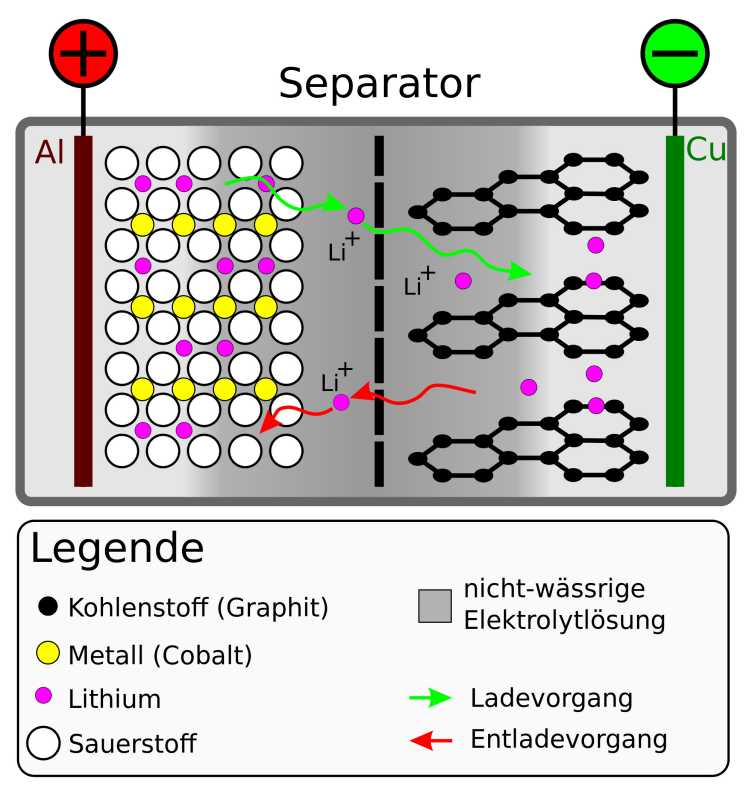
Une batterie lithium-ion actuelle est composée de deux électrodes - une cathode et une anode. L'anode est souvent composée de graphite, la cathode d'oxydes métalliques comme l'oxyde de cobalt. C'est dans ces matériaux que les ions de lithium se nichent lors de la charge ou de la décharge. Les deux électrodes sont séparées par une cloison qui ne laisse passer que les ions de lithium. Lors de la décharge, les ions lithium se déplacent de l'anode vers la cathode. Les électrons de ce dernier ne passent pas à travers la paroi de séparation et font donc un détour par un appareil électronique qui est alimenté par le courant d'électrons qui en résulte. Les électrons et les ions se rencontrent à nouveau à la cathode. Lors de la charge, les ions et les électrons sont forcés de circuler dans le sens inverse. Pour qu'une batterie fonctionne bien et longtemps, les ions doivent pouvoir se déplacer facilement dans et hors des matériaux des électrodes. La forme et la taille du matériau de l'électrode ne doivent pas non plus être modifiées de manière significative par l'absorption et la libération répétées des ions.
Référence bibliographique
He M, K Kravchyk, Walter M, Kovalenko MV : Nanocristaux d'antimoine monodisperses pour anodes de batteries Li-ion et Na-ion à haut rendement : Nano versus Bulk. Nano Lett. 31 janvier 2014. DOI : page externe10.1021/nl404165c