Une meilleure résolution grâce à l'hyperpolarisation
Un article qui vient d'être publié dans la revue Proceedings of the National Academy of Sciences (PNAS) présente une nouvelle méthode d'IRM. Le secret de cette nouvelle méthode réside dans les matériaux dits hyperpolarisants ou HYPSO en abrégé. Le co-auteur de l'étude, le professeur de l'ETH Christophe Copéret, explique le mode d'action de cette nouvelle méthode.
Les méthodes d'imagerie telles que l'imagerie par résonance magnétique (IRM) ou la tomodensitométrie (CT) sont devenues incontournables dans la médecine actuelle. Ces méthodes permettent des diagnostics plus rapides et plus précis et se sont considérablement améliorées au cours des dernières années. Cependant, en raison de la complexité du corps humain, la résolution et la qualité des images limitent encore ces technologies. Une collaboration entre des chercheurs de l'ETH Zurich, de l'EPFL, du CNRS, de l'ENS Lyon, du CPE Lyon ont mis en place un page externenouvelle approche pour améliorer considérablement les possibilités d'imagerie médicale tout en augmentant la sécurité des patients.
Actualités ETH : Que faut-il s'imaginer sous HYPSO ?
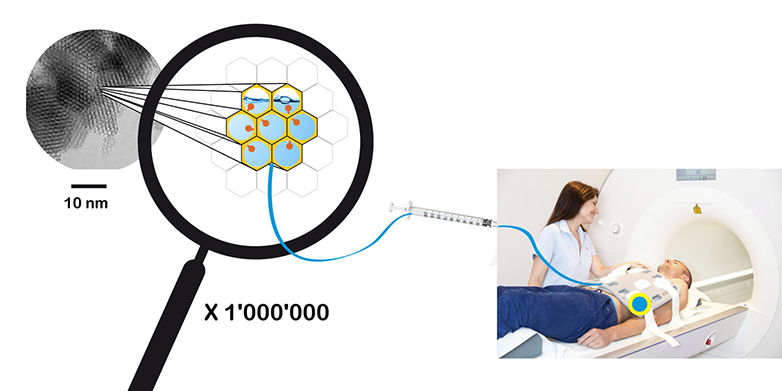
Christophe Copéret : Les HYPSO sont une nouvelle génération de matériaux permettant de polariser les molécules en solution, c'est-à-dire que les spins nucléaires sont tous orientés de la même manière. Ces matériaux se présentent sous la forme d'une fine poudre blanche et sont composés de silicate, le principal composant du sable. Il a été conçu de manière à présenter de nombreux pores d'un diamètre compris entre cinq et dix nanomètres. Des radicaux organiques, véritable source de polarisation, sont déposés uniformément à la surface du silicate. Ces matériaux nous ont permis de polariser des métabolites importants pour l'imagerie par résonance magnétique 13-C.
Quels sont les avantages de la nouvelle procédure ?
Dans l'IRM "classique", telle qu'elle est utilisée aujourd'hui de manière standard, le signal provient des protons dans l'eau. Il en résulte une bonne sensibilité, mais le contenu informatif n'est pas très élevé. Par exemple, les tumeurs doivent être relativement grosses pour être détectées par IRM classique. Certaines tumeurs qui ne changent pas de taille sont malheureusement détectées beaucoup trop tard. L'avantage de l'IRM C-13 par rapport à l'IRM classique est qu'elle permet de détecter les produits du métabolisme et leur concentration dans le corps. Comme les cellules cancéreuses ont des taux de métabolisation différents de ceux des cellules saines, la concentration donne des informations directes sur l'état des tissus, indépendamment de la taille d'une tumeur. L'IRM C-13 a toutefois une sensibilité beaucoup plus faible que l'IRM classique. C'est pourquoi les métabolites doivent être polarisés pour pouvoir être détectés. Aujourd'hui, les méthodes de polarisation reposent sur des radicaux en solution qui ne doivent pas pénétrer dans le corps et qui sont donc éliminés avant l'IRM. Cette séparation prend un certain temps. Comme la polarisation se désagrège au bout de quelques secondes, on perd en fin de compte une précieuse résolution dans les images.
En revanche, nos matériaux peuvent être facilement et rapidement retirés de la solution polarisée par filtration. Ainsi, nous sommes en mesure d'enregistrer des spectres de la solution hyperpolarisée. Nous espérons que notre matériel contribuera à faire de l'IRM C-13 une méthode standard.
Comment fonctionnent les HYPSO ?
Les canaux des pores sont remplis d'une solution d'une molécule spécifique, dans notre cas le pyruvate. Ceci est physiologiquement important, car le pyruvate est très rapidement dégradé en lactate dans les cellules cancéreuses. L'isotope de carbone C-13, un isotope non radioactif naturellement présent dans tous les tissus vivants et dans les produits métaboliques, est "polarisé". Après la polarisation à basse température, tout est décongelé, la solution est filtrée et peut ensuite être détectée par IRM au C-13.
Quelle a été votre contribution à l'ETH Zurich pour cette étude ?
Mon groupe à l'ETH Zurich a développé les HYPSO en collaboration avec CPE Lyon. La principale difficulté a été d'obtenir le contrôle de la répartition des radicaux le long des pores du silicate très poreux. Une répartition uniforme des radicaux est indispensable pour notre application et repose sur la collaboration entre chimistes et scientifiques des matériaux. À l'EPF de Lausanne, les chercheurs ont construit les instruments nécessaires à cette technique et l'ENS Lyon a coordonné le projet.
Qui a eu l'idée d'utiliser de la poudre de silicate comme agent de polarisation ?
Nous travaillons depuis un certain temps déjà avec de tels matériaux et les utilisons pour le développement de catalyseurs hétérogènes. Grâce à ce projet, nous avons maintenant appris à contrôler la répartition des centres actifs à la surface. Parallèlement, nous avons récemment développé une nouvelle technique pour caractériser la surface de ces matériaux par résonance magnétique nucléaire (RMN) (Surface Enhanced NMR Spectroscopy - SENS). Pour ce faire, nous utilisons à chaque fois une solution de radicaux organiques pour polariser la surface. Nous nous sommes demandés si nous pouvions également inverser la situation et polariser une solution avec un corps solide.
Combien de temps a duré le développement du matériau et de l'application ?
Même pas deux ans, car nous étions bien préparés à cette problématique grâce à nos recherches sur les catalyseurs. Nous avons "simplement" dû adapter notre méthode et bien sûr tester divers matériaux. Finalement, nous pouvons expliquer quels matériaux fonctionnent le mieux sur les appareils de l'EPFL.
Quelles sont les prochaines étapes de ce projet ?
Jusqu'à présent, nous avons montré que nos matériaux fonctionnent et nous voulons clairement développer le procédé pour une utilisation en IRM. Nous étudions actuellement de nouveaux types d'HYPSO qui permettent une polarisation encore plus élevée.
Quand les HYPSO seront-elles disponibles en médecine ?
Nous y travaillons également actuellement. J'espère que nous parviendrons à faire entrer les HYPSO dans la clinique dans les années à venir.
A propos de la personne
Christophe Copéret est professeur ordinaire de chimie inorganique au Département de chimie et des sciences biologiques appliquées (D-CHAB) de l'ETH Zurich depuis novembre 2010. Il s'intéresse à la chimie des molécules, des matériaux et des surfaces dans le but de développer des matériaux fonctionnels utilisés dans la catalyse, la reconnaissance moléculaire, l'imagerie et la microélectronique.
Référence bibliographique
Gajan D, Bornet A, Vuichoud B, Milani J, Melzi R, van Kalkeren HA, Veyre L, Thieuleux C, Conley MP, Grüning WR, Schwarzwälder M, Lesage A, Copéret C, Bodenhausen G, Emsley L, Jannin S. Hybrid polarizing solids for pure hyperpolarized liquids through dissolution dynamic nuclear polarization. PNAS 29 septembre 2014. DOI : page externe10.1073/pnas.1407730111