Contrôler les gènes par la pensée
Des chercheurs de l'ETH menés par Martin Fussenegger ont mis au point le premier réseau de gènes qui se met en marche grâce aux ondes cérébrales et qui produit différentes quantités d'une molécule souhaitée en fonction des pensées. Ils se sont inspirés d'un jeu qui capte également les ondes cérébrales pour guider une balle à travers un parcours d'obstacles.
On se croirait presque dans la saga spatiale "Star Wars", où Maître Yoda enseigne au jeune Luke Skywalker comment sortir le X-Wing Starfighter des marais par la force de la pensée : Marc Folcher ainsi que d'autres chercheurs du groupe de Martin Fussenegger, professeur de biotechnologie et de génie biologique au Département des systèmes biologiques (D-BSSE) à Bâle, ont mis au point une méthode de régulation génétique d'un genre nouveau, dans laquelle les pensées - ou plutôt les ondes cérébrales spécifiques qu'elles génèrent - contrôlent la conversion des gènes en protéines, appelée expression dans le jargon scientifique.
"Pour la première fois, nous avons réussi à capter des ondes cérébrales humaines, à les transmettre sans fil à un réseau de gènes et à réguler l'expression d'un gène, en fonction de la nature des pensées. Le contrôle de l'expression des gènes par le pouvoir de la pensée était un rêve que nous poursuivions depuis plus d'une décennie", explique Fussenegger.
Le jeu "Mindflex" a été une source d'inspiration pour le nouveau système de régulation génétique contrôlé par la pensée. Dans ce jeu, un joueur porte une sorte d'écouteur avec un capteur sur le front qui enregistre les ondes cérébrales. L'électroencéphalogramme (EEG) enregistré est ensuite transmis à l'environnement de jeu. L'EEG contrôle un ventilateur pour guider une petite balle à travers un parcours d'obstacles.
Transmission sans fil sur implant
Le système que les bio-ingénieurs bâlois viennent de présenter dans "Nature Communications" consiste désormais également en un casque EEG. Les ondes cérébrales captées sont évaluées et transmises sans fil via Bluetooth à un contrôleur. Celui-ci commande un générateur de champ qui produit un champ électromagnétique alimentant un implant en courant par induction.
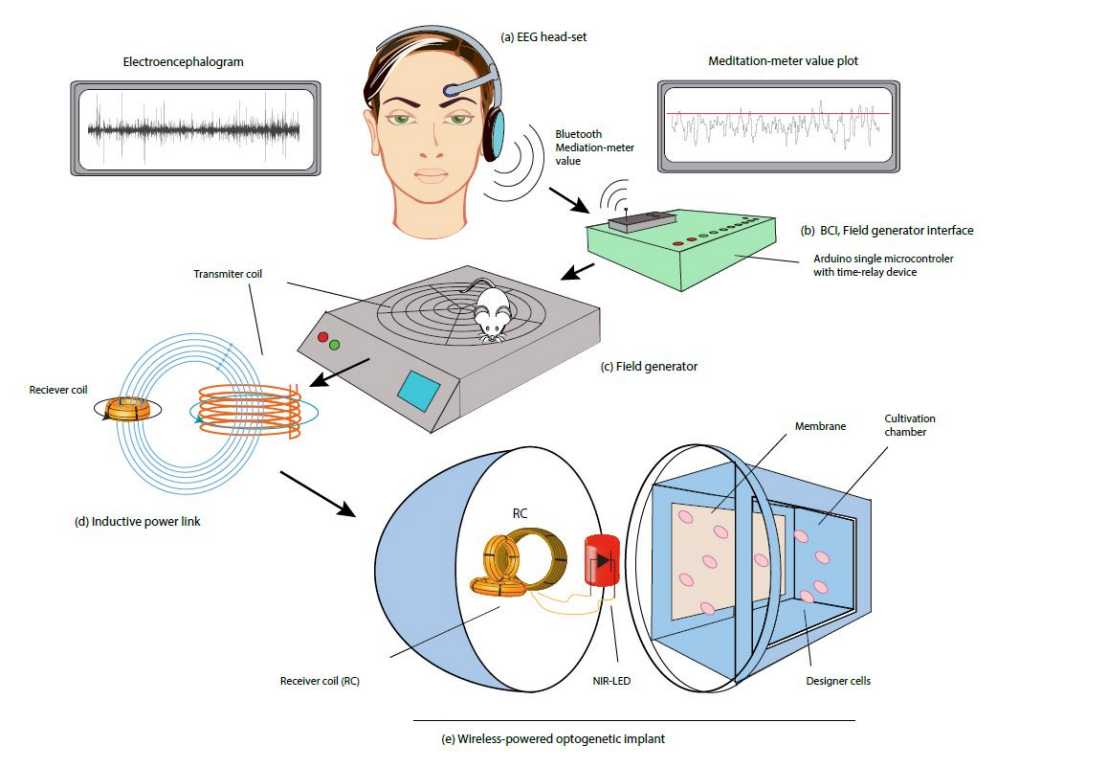
Une lumière s'allume ensuite littéralement dans l'implant : Une petite lampe LED intégrée, qui émet de la lumière dans le proche infrarouge, s'allume et éclaire une chambre de culture contenant des cellules génétiquement modifiées. Dès que la lumière proche infrarouge éclaire les cellules, celles-ci commencent à produire la protéine souhaitée.
La pensée contrôle la quantité de protéines
L'implant a d'abord été testé dans des cultures cellulaires et chez des souris, guidé par les pensées de différents sujets. Dans leurs tests, les chercheurs ont travaillé avec SEAP, un modèle de protéine humaine facile à détecter, qui se diffuse de la chambre de culture de l'implant dans la circulation sanguine de la souris.
Pour réguler la quantité de protéines libérées, les sujets devaient se mettre dans trois états de pensée différents : Biofeedback, méditation et concentration. Les sujets qui jouaient à Minecraft sur l'ordinateur, c'est-à-dire qui se concentraient, induisaient des valeurs moyennes de SEAP dans la circulation sanguine des souris, tandis qu'en état de relaxation totale, c'est-à-dire de méditation, des valeurs sanguines très élevées de SEAP étaient atteintes chez les animaux de laboratoire. Lors du biofeedback, les sujets observaient la lumière LED de l'implant dans le corps de la souris et pouvaient, grâce à cette rétroaction visuelle de leurs pensées, allumer ou éteindre consciemment la lumière LED le plus longtemps possible. Cela se traduisait à son tour par des quantités variables de SEAP dans la circulation sanguine des animaux.
Nouvelle construction génétique sensible à la lumière
"Un tel contrôle des gènes est complètement nouveau et unique dans sa simplicité", explique M. Mussenegger. Le module optogénétique sensible à la lumière, qui réagit à la lumière infrarouge proche, est notamment un nouveau développement. La lumière atteint une protéine photosensible modifiée à l'intérieur de cellules génétiquement modifiées et y déclenche une cascade de signaux artificiels, à la fin de laquelle se produit la production de SEAP. Le proche infrarouge a été utilisé parce qu'il est largement inoffensif pour les cellules humaines, qu'il peut pénétrer profondément dans les tissus et qu'il permet de suivre visuellement le fonctionnement de l'implant.
Le système existant fonctionne parfaitement dans les systèmes homme-culture cellulaire et homme-souris. Fussenegger espère qu'un implant contrôlé par la pensée pourrait un jour aider à détecter précocement des maladies neurologiques comme les maux de tête et de dos chroniques ainsi que l'épilepsie grâce à des ondes cérébrales spécifiques. Cela permettrait de déclencher et de contrôler la formation en temps voulu de certaines substances actives dans les implants mis en place.
Référence bibliographique
Folcher M, Oesterle S, Zwicky K, Thekkottil T, Heymoz J, Hohmann M, Christen M, Daoud El-Baba M, Buchmann P, Fussenegger, M : Mind-controlled transgene expression by a wireless-powered optogenetic designer cell implant. Nature Communications, publication en ligne du 11 novembre 2014, doi : page externe10.1038/ncomms6392